Адрес этой статьи в интернете: www.biophys.ru/archive/sarov2013/proc-p18.htm
Спин-изомеры Н2О в реакционном центре фотосинтезирующих пурпурных бактерий
Пищальников Р.Ю., Першин С.М., Бункин А.Ф.
Научный Центр Волновых Исследований ИОФРАН им А.М.Прохорова,
119991, Россия, Москва, ул. Вавилова 38, E-mail: rpishchal@kapella.gpi.ru
ВВЕДЕНИЕ
Ключевой проблемой понимания фотосинтеза является определение механизма управления электронным транспортом в реакционных центрах (РЦ) светособирающих комплексов растений и бактерий. Мы обратили внимание на энергетические особенности орто-пара изомеров Н2О, которые должны проявляться в изолированном состоянии уединенных мономеров Н2О, входящих в состав РЦ пурпурных бактерий. Ранее нами была сформулирована гипотеза о влиянии этих молекул воды на миграцию электрона [1] и проведен квантовомеханический расчет модуляции кинетики [2].
Известно [3], что РЦ пурпурных бактерий, ответственные за транспорт электрона и разделение заряда, содержат две молекулы воды. Роль последних остается пока неясной. Ещё до появления рентгеноструктурных данных по РЦ, насколько нам известно, авторы предположили [4], что молекулы Н2О выполняют управляющую роль посредством дипольного взаимодействия с окружением. Кроме отдельных упоминаний [5], это предположение не получило поддержки и дальнейшего развития. Позднее [3, 6] методом рентгеноструктурного анализа было уточнено местоположение молекул Н2О в реакционном центре. Далее в [7-9] удалось зарегистрировать модуляцию кинетики при зондировании - накачке на гига- и терагерцовых частотах, которые в [9, 10] авторы интерпретировали как частоты вращения молекул Н2О (или D2O) без обсуждения механизма. Квантово-механический расчёт стимулированного излучения и поглощения из возбуждённого состояния в диапазоне 850–1050 нм проводился в [11]. Однако, магнитные свойства молекул орто-Н2О (D2O) как носителей ненулевого магнитного момента не принимались во внимание до настоящего времени, несмотря на серию работ с обсуждением спиновых механизмов управления электронным [12-14] и протонным транспортом [15].
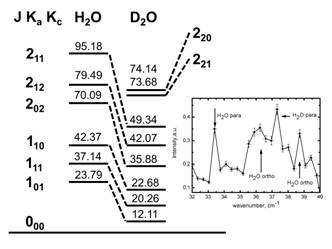
Методом низкочастотной четырехфотонной спектроскопии нами были обнаружены вращения мономеров Н2О в воде [16-19]. Вращательные резонансы Н2О были отнесены к орто (суммарный магнитный момент протонов равен 1, триплет) и пара (суммарный магнитный момент равен 0, синглет) спин-изомерам Н2О. Была установлена также спин-селективная избирательность связывания молекул пара-Н2О биополимерами при их гидратировании в водных растворах [20] с одновременным увеличением интенсивности линий орто-Н2О. На рис. 2 показан фрагмент спектра четырёхфотонного рассеяния в воде на вращательных переходах орто-H2O: 36,6 см-1 (312-303), 38,8 см-1, а также пара-H2O: 33,4 (211-202), 37,1 см-1 (111-000) [21].
|
|
|
Рисунок 1. РЦ пурпурных бактерий (овал) в окружении молекулы H2O. Составные части РЦ: Pa, Pb, BChl Ba, BChl Bb – 4 молекулы бактериохлорофилла; BPheo Ha, BPheo Hb – 2 молекулы бактериофеофетина и Qa, Qb – 2 молекулы хинона. [45] |
|
|
|
Рисунок 2. Слева показана схема
вращательных уровней молекул H2O и D2O в
основном колебательном состоянии для |
Наши измерения вращательных переходов молекул Н2О методом КР и выводы о вращении молекул Н2О в воде и водных растворах биополимеров на основе четырехфотонной спектроскопии [16-18, 20, 22] не противоречат экспериментальным данным [7-10, 23, 24] о модуляции кинетики стимулированного излучения РЦ на частотах вращения молекул Н2О. В [9, 25] наблюдаемая модуляция интерпретировалась как проявление обертонов вращательного перехода Н2О основного тона 9 см-1 на частотах 15, и 30 см-1. Однако, оставалось неясным, почему модуляция кинетики происходит именно на этом тоне и его обертонах. В [11] эти частоты не были соотнесены с какими-либо конкретными переходами.
Вращательные резонансы орто и пара спин-изомеров Н2О были обнаружены нами и во льдах [26]. Каналы гексагонального льда рассматриваются нами как полости [27-29], в которых мономеры свободно вращаются, как, например, в полостях аргонового льда [30].
Цель данной работы - количественное обоснование связи модуляции электронного транспорта в первичных процессах фотосинтеза с возбуждением вращательных уровней спин-изомеров орто-D2О (эта модуляция была обнаружена в [9, 10]). Гипотетическая возможность этой связи была сформулирована нами ранее [1]. Был проведен также квантово-механический расчет для молекулы Н2О [2].
МАТЕРИАЛЫ И МЕТОДЫ
Вычисления и построение функциональных зависимостей проводились с помощью пакета программ MATLAB, а также программ, разработанных нами в среде программирования Visual Studio 2010 на языке C++. Информация о пространственной структуре РЦ, выделенного из Rba. Sphaeroides, была получена из базы the Protein Data Bank (www.pdb.org). Для визуализации молекул и графической информации использовалась программа PyMol 0.99. Структура энергетических уровней для молекулы H2O была получена из базы данных HITRAN [31], а для молекулы D2O - из монографии [32].
Результаты экспериментов по накачке-зондированию фемтосекундными импульсами, выполненные на мутантах РЦ из Rba. Sphaeroides для сравнения с расчётными параметрами и зависимостями, были взяты из [9, 10].
МОДЕЛЬ И ТЕОРИЯ
РЦ светособирающей антенны пурпурных бактерий состоит из четырёх молекул бактериохлорофилла (БХл), двух молекул бактериофеофетина (БФео), молекулы каротиноида, двух молекул хинона и атома негемового железа [3, 6, 33]. Пространственная структура РЦ, определённая методом рентгеновского структурного анализа, описана в [3, 6]. Молекулы РЦ организованы в две симметричные ветви (A и B). Основание РЦ образует димер близкорасположенных плоскопараллельных молекул БХл Pa и Pb, который называется специальной парой (СП) P (рис.1, 3 и 4). Далее БХл Ba и Bb, БФео Ha и Hb, а также молекулы хинонов Qa и Qb образуют две ветви РЦ. Атом железа Fe располагается между хинонами в фиксированном положении (см. рис. 6). Перенос электрона начинается после перехода СП в синглетное возбуждённое состояние P*. В течение примерно 3 пс формируется состояние P+B-, далее за 1 пс P+B- релаксирует к долгоживущему состоянию P+H-, которое за 200 пс формирует состояние P+Qa-. Данные времена соответствуют комнатной температуре образцов.
|
|
|
Рисунок 3. Расположение молекул СП, БХл Ba и Bb, молекул H2O и гистидина His M202 в РЦ. Отмечены расстояния (в ангстремах) между молекулой H2O и ближайшими атомами окружения. [45] |
|
|
|
Рисунок 4. Схема уровней энергии, соответствующая состояниям с разделёнными зарядами PB, P*B, P+B- и P+(B-)* в РЦ, где Hg, H1, He2 и Hf – многообразие возбуждённых состояний вращательных и колебательных уровней. Вертикальными стрелками обозначены основные переходы задействованные в эксперименте зондирования и накачки. Горизонтальными стрелками обозначены близкорасположенные уровни орто-пара переходов молекулы воды. [46] |
Сопоставляя наши данные КР о вращении орто/пара Н2О в воде (рис. 2) и водных растворах белков [16-18, 20, 22], а также данные рентгеноструктурного анализа (рис. 3), мы предположили, что эти молекулы могут вращаться и различаться (или совпадать) по спиновому состоянию. Наблюдаемая асимметрия правой и левой половины молекулярного комплекса РЦ, скорее всего, обусловлена тем, что размещения молекулы Н2О в этих ветвях различаются расстоянием до окружающих её комплексов [34]. Существенно, что минимальное из этих расстояний (7,23 А, 4,40 А, 3,28 А), заметно больше длины водородной связи (2,98 А) в (Н2О)2, что позволяет молекуле свободно вращаться как бы в «эквипотенциальной полости».
Схема эволюции энергетических уровней состояний с разделёнными зарядами в реакционном центре пурпурных бактерий [9, 11] представлена на рис. 3. Возбуждение СП P→P* инициирует процесс переноса электрона на Бхл Ba. Образуемое состояние P+B- может переходить в возбуждённое состояние P+(B-)*. Таким образом, исследуемая система имеет четыре электронных уровня: основной (PB), два одно-экситонных (P*B и P+B-) и один двух-экситонный (P+(B-)*). Согласно нашей гипотезе, каждый из этих уровней взаимодействует с колебательными модами молекул пигментов и колебательно-вращательными модами молекул H2O, расположенными в РЦ.
Для моделирования динамики состояний с разделёнными зарядами используем стандартную теорию, описывающую эволюцию матрицы плотности в пространстве Лиувилля [11, 35, 36].
Полную энергию системы удобно представить в виде:
![]() (1)
(1)
Волновые функции экситонных состояний (рис. 3) обозначаем далее как ![]() для
(PB),
для
(PB), ![]() и
и ![]() для (P*B) и (P+B-) и
для (P*B) и (P+B-) и ![]() для (P+(B-)*), тогда
для (P+(B-)*), тогда
![]() . (2)
. (2)
Для электронных состояний определим множество колебательно-вращательных подуровней. Пренебрегая эффектами центробежного искажения, кориолисова взаимодействия колебаний и ангармоничности, колебательно-вращательный гамильтониан из [37, 38] получаем в виде:
![]() .
(3)
.
(3)
Здесь ![]() -
нормальные координаты,
-
нормальные координаты, ![]() - сопряжённые с ними импульсы;
- сопряжённые с ними импульсы; ![]() (cm-1);
(cm-1); ![]() -
компоненты углового момента по молекулярно-фиксированным осям;
-
компоненты углового момента по молекулярно-фиксированным осям; ![]() -
компоненты обратного тензора инерции для равновесной конфигурации молекулы
[37]. Стационарное уравнение Шредингера имеет вид:
-
компоненты обратного тензора инерции для равновесной конфигурации молекулы
[37]. Стационарное уравнение Шредингера имеет вид:
![]() .
(4)
.
(4)
В (4) возможно разделение вращательных и колебательных переменных [38]:
![]() (5)
(5)
![]()
Здесь ![]() -
углы Эйлера,
-
углы Эйлера, ![]() - моды нормальных колебаний
молекулы воды, где
- моды нормальных колебаний
молекулы воды, где ![]() . Колебательный гамильтониан для
изолированной молекулы воды имеет вид:
. Колебательный гамильтониан для
изолированной молекулы воды имеет вид:
![]() ,
(6)
,
(6)
![]() - частоты нормальных
колебаний молекулы воды, где
- частоты нормальных
колебаний молекулы воды, где ![]() ,
, ![]() -
нелинейные поправки к модели гармонического осциллятора,
-
нелинейные поправки к модели гармонического осциллятора, ![]() -
собственные функции колебательных состояний [39].
-
собственные функции колебательных состояний [39].
Вращательные уровни изолированной молекулы воды вычисляются в приближении жесткого асимметричного волчка:
![]() ,
(7)
,
(7)
где ![]() -
вращательные постоянные. Индексы a, b и с
отмечают главные оси инерции. В общем случае значения собственных
вращательных энергий и собственных вращательных функций определяются тремя
квантовыми числами: J=0, 1, 2,…; k=±0, 1, 2,…, ±J; m=±0, 1, 2,…, ±J. Для молекулы, относящейся к типу
асимметричного волчка, ненулевыми являются те матричные элементы, для которых J
и m одинаковы, а также матричные
элементы с одинаковыми либо отличающимися на 2 значениями k. Для молекулы воды набор
квантовых чисел обозначается как J, Ka
и Kc. На рисунке 1 приведены значения
энергий первых вращательных уровней для основного колебательного состояния
молекул Н2О и D2O. Видно, что наличие нейтрона в
молекуле D2O и увеличение момента инерции проявляется в уменьшении
энергии вращательных термов по сравнению с молекулой Н2О при
одинаковых значениях квантовых чисел уровней.
-
вращательные постоянные. Индексы a, b и с
отмечают главные оси инерции. В общем случае значения собственных
вращательных энергий и собственных вращательных функций определяются тремя
квантовыми числами: J=0, 1, 2,…; k=±0, 1, 2,…, ±J; m=±0, 1, 2,…, ±J. Для молекулы, относящейся к типу
асимметричного волчка, ненулевыми являются те матричные элементы, для которых J
и m одинаковы, а также матричные
элементы с одинаковыми либо отличающимися на 2 значениями k. Для молекулы воды набор
квантовых чисел обозначается как J, Ka
и Kc. На рисунке 1 приведены значения
энергий первых вращательных уровней для основного колебательного состояния
молекул Н2О и D2O. Видно, что наличие нейтрона в
молекуле D2O и увеличение момента инерции проявляется в уменьшении
энергии вращательных термов по сравнению с молекулой Н2О при
одинаковых значениях квантовых чисел уровней.
|
|
|
Рисунок 5. Локализация состояний P* и (P+B-) в РЦ. [45] |
|
|
|
Рисунок 6. Результат квантовомеханического расчета спонтанного излучения (SE) (зависимость на 970 нм) и поглощения из возбуждённого состояния (ESA) (зависимость на 1130 нм) с учётом одной моды колебательных состояний для H1, He2 и Hf и вращательных уровней молекулы H2O (слева) и D2O (справа) для гамильтониана Hg. [45] |
Таким образом,
колебательно-вращательное возбуждённое состояние молекулы воды определяется
набором из 6 квантовых чисел: ν1, ν2, ν3,
J, Ka, Kc. С учётом условий симметрии, налагаемых на
волновую функцию колебательно-вращательных состояний молекулы воды [38],
состояния ![]() могут быть классифицированы по
следующему правилу: если ν3+Ka+Kc нечетно, то
могут быть классифицированы по
следующему правилу: если ν3+Ka+Kc нечетно, то ![]() -
орто-состояние, а если чётно, то
-
орто-состояние, а если чётно, то ![]() -
пара-состояние. Заметим, что
для молекулы D2O классификация изомеров по квантовым числам отличается:
нечётная сумма соответствует пара-, а чётная сумма – орто-состоянию.
-
пара-состояние. Заметим, что
для молекулы D2O классификация изомеров по квантовым числам отличается:
нечётная сумма соответствует пара-, а чётная сумма – орто-состоянию.
Вычисление
оптического отклика в эксперименте «зондирования-накачки» включает расчёт релаксационных
кинетик для населённостей
оптически возбуждаемых электронных состояний ![]() ,
, ![]() и
и
![]() . Каждому электронному состоянию
соответствует подмножество колебательно-вращательных уровней (рисунок 2). В
нашей модели гамильтониан
. Каждому электронному состоянию
соответствует подмножество колебательно-вращательных уровней (рисунок 2). В
нашей модели гамильтониан ![]() вычисляется с
учётом близкорасположенных орто-пара состояний
молекулы воды, а
вычисляется с
учётом близкорасположенных орто-пара состояний
молекулы воды, а ![]() ,
, ![]() и
и ![]() -
способом, описанным в [11].
-
способом, описанным в [11].
Для каждого из гамильтонианов
![]() ,
,![]() ,
,![]() и
и
![]() решается задача на собственные
значения и собственные векторы экситонных состояний.
Далее вычисляются дипольные моменты для переходов
решается задача на собственные
значения и собственные векторы экситонных состояний.
Далее вычисляются дипольные моменты для переходов ![]() (
(![]() ),
),
![]() (
(![]() ),
), ![]() (
(![]() )
и
)
и ![]() (
(![]() ) в экситонном приближении.
) в экситонном приближении.
![]() ,
, ![]() ,
(8)
,
(8)
![]() ,
, ![]() .
.
здесь ![]() ,
,![]() и
и ![]() - состояния, соответствующее
основному, одно - и двух- экситонным
возбуждениям. Эволюция системы описывается квантовым уравнением Лиувилля для редуцированной матрицы плотности
- состояния, соответствующее
основному, одно - и двух- экситонным
возбуждениям. Эволюция системы описывается квантовым уравнением Лиувилля для редуцированной матрицы плотности ![]() :
:
![]() ,
(9)
,
(9)
Здесь ![]() -
оператор Редфилда [40], описывающий релаксационные
процессы в пределе слабого взаимодействия электронных, колебательных и
вращательных мод с окружением. Решение уравнения ищется в виде
-
оператор Редфилда [40], описывающий релаксационные
процессы в пределе слабого взаимодействия электронных, колебательных и
вращательных мод с окружением. Решение уравнения ищется в виде ![]() ,
то есть, в виде суммы по трём порядкам теории возмущений. Здесь
,
то есть, в виде суммы по трём порядкам теории возмущений. Здесь ![]() -
оператор, описывающий воздействие внешнего поля на систему. Его вид
определяется типом эксперимента. Моделируемые экспериментальные данные динамики
состояний с разделёнными зарядами исследовались методом зондирования и накачки
[40], для которого
-
оператор, описывающий воздействие внешнего поля на систему. Его вид
определяется типом эксперимента. Моделируемые экспериментальные данные динамики
состояний с разделёнными зарядами исследовались методом зондирования и накачки
[40], для которого
![]() , (10)
, (10)
![]()
Здесь
![]() и
и ![]() - единичные
векторы, определяющие поляризацию импульсов накачки и зондирования;
- единичные
векторы, определяющие поляризацию импульсов накачки и зондирования; ![]() ,
,
![]() и
и ![]() ,
, ![]() -
частоты и волновые векторы импульсов;
-
частоты и волновые векторы импульсов; ![]() - форма
импульса;
- форма
импульса; ![]() - задержка; символы
- задержка; символы ![]() и
и
![]() обозначают эрмитово
сопряжённые и комплексно сопряжённые части выражений для
обозначают эрмитово
сопряжённые и комплексно сопряжённые части выражений для ![]() и
и ![]() .
.
Регистрируемый сигнал описываем равенствами:
![]() ,
(11)
,
(11)

где ![]() -
поляризация среды в третьем порядке теории возмущения.
-
поляризация среды в третьем порядке теории возмущения.
Расчёт эволюции
поляризации проводился в предположении, что длительности возбуждающего и
зондирующего импульсов малы по сравнению с характерными временами когерентности
для экситонных переходов ![]() и
и ![]() .
Расчёт амплитуды стимулированного излучения
.
Расчёт амплитуды стимулированного излучения ![]() и
поглощения из возбуждённого состояния
и
поглощения из возбуждённого состояния ![]() проводился в
импульсном режиме [11, 40].
проводился в
импульсном режиме [11, 40].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Анализ Фурье-спектра из [11] показал, что вычисленные значения энергий в пределах спектрального разрешения 4 см-1 соотносятся с вращательными линиями орто-пара изомеров Н2О (таблица 1). В первой колонке таблицы даны значения частот из [11], во второй и четвертой – частоты переходов Н2О и энергии уровней из базы данных HITRAN [31]. Наклонным шрифтом отмечены частоты переходов пара–изомера Н2О с нулевым спином. Из сравнения первой и второй колонок таблицы 1 видно, что измеренные в [11] линии переходов хорошо совпадают с истинными вращательными линиями орто-пара Н2О и, скорее всего, не являются обертонами, как предполагалось в [11]. Аналогично была составлена таблица 2 для вращательных уровней основного колебательного состояния молекулы D2О.
В табл.1 включены до двух десятков резонансных переходов из тысячи вращательных линий Н2О в основном колебательном состоянии в диапазоне до 300 см-1 [31]. При выборе этих переходов мы руководствовались условием образования смешанных квантовых состояний орто-пара изомеров Н2О. Известно [41], что критерием образования смешанных квантовых состояний, в которых вероятность орто-пара конверсии возрастает, является разность энергий близко расположенных верхних или нижних орто-пара уровней. В соответствии с этим критерием, которому удовлетворяют близко расположенные уровни в правой колонке таблицы 1 с разностями энергий порядка 1 см-1 и менее того, набор вращательных линий [31] сильно прореживается.
Таблица 1. Сравнение вращательных орто/пара уровней молекулы D2O из базы данных HITRAN [31] с результатами Фурье-анализа данных эксперимента [11]. Толстым шрифтом выделены орто-пара уровни, имеющие близко расположенные уровни, вместе с которыми образуют смешанные квантовые состояния и обеспечивают орто-пара конверсию в окрестности катализатора.
|
Моды фурье спектра, cm-1 |
Вращательные орто/пара уровни D2O, [32], cm-1 |
Уровни переходов |
Энергия близких орто-пара уровней, cm-1 |
|
9 |
8,8069 8,8518 8,8414 |
10 3 8→ 10 2 8 11 7 4→10 8 3 11 7 5→10 8 2 |
108 2 =1242.01 108 3 =1242.01 117 5 =2321.81 117 4 =2321.91
|
|
24 |
24,1063 24,2216 24,1021 |
5 2 3→4 3 2 11 5 7→12 2 10 14 3 12→13 4 9 |
4 3 2=205.89 4 3 1=206.28 142 12=1330.52 143 12=1331.40 |
|
72 |
71,8813 72,0136 |
5 2 3→4 2 3 7 3 4→7 1 6 |
|
|
96 |
96,2426 |
4 3 1→3 2 2 |
4 3 2=205.89 4 3 1=206.28 |
|
123 |
122,7551 122,8921 122,9221 |
7 4 4→7 2 6 15 4 12→14 7 8 15 4 12→14 6 8 |
7 4 4= 492.02 7 4 3= 492.88 |
|
148 |
147,9660 148,1569 148,0727 |
7 3 4 6 2 5 9 2 7→8 6 3 12 3 10→13 2 11 |
8 6 3= 767.72 8 6 2=767.72
|
|
187 |
187,3730 187,1130
|
7 4 3→7 0 7 7 4 4→7 1 7 |
7 4 4= 492.02 7 4 3= 492.88 7 0 7= 305.50 7 1 7= 305.77 |
|
324 |
324,0768 324,0768 |
10 7 3→10 3 7 10 7 3→10 3 7 |
10 7 4= 1114.89 10 7 3= 1114.89 |
Рассматриваемый механизм конверсии в смешанных квантовых состояниях дает основание предположить, что в совокупности РЦ, которые попадают в область пересечения пучка накачки и пробного пучка, присутствует какая-то доля изолированных орто-Н2О молекул. Эта доля может превышать 75% от числа всех изолированных молекул в этом объеме (в соответствии с равновесным отношением орто:пара=3:1 до температур ~40 K, которое определяется квантовой статистикой [16, 41]). Ясно, что любое отклонение от равновесного отношения орто/пара будет приводить к неравновесному состоянию переохлаждения (либо перегрева) по спиновой температуре и к локальной неустойчивости.
Имея в виду
гипотезу, сформулированную нами ранее [1], мы провели квантово-механический
расчет кинетики флюоресценции РЦ, схема которого изложена выше. В отличие от
[11], где аналогичный расчет был проведён без какого-либо отнесения частот
переходов, в нашем расчёте собственные значения гамильтониана ![]() соответствуют
уровням вращательных переходов из правой колонки таблицы 1 и таблицы 2.
соответствуют
уровням вращательных переходов из правой колонки таблицы 1 и таблицы 2.
Результат
моделирования стимулированного излучения и поглощения из возбуждённого
состояния представлен на рис. 6. Значения энергий переходов ![]() ,
, ![]() ,
,
![]() и
и ![]() выбирались
так, чтобы воспроизвести положения основных пиков поглощения 870 нм и 1020 нм.
Гамильтониан
выбирались
так, чтобы воспроизвести положения основных пиков поглощения 870 нм и 1020 нм.
Гамильтониан ![]() был сформирован с использованием
значений энергий из таблицы 1. Гамильтонианы
был сформирован с использованием
значений энергий из таблицы 1. Гамильтонианы ![]() ,
, ![]() и
и
![]() формировались на основе модели
гармонического осциллятора с учётом изменения потенциальной энергии для каждого
экситонного состояния [11]. Полученные модуляции для
молекул Н2О (рис. 6 слева) и D2O (рис 6 справа)
качественно соответствуют экспериментальным данным.
формировались на основе модели
гармонического осциллятора с учётом изменения потенциальной энергии для каждого
экситонного состояния [11]. Полученные модуляции для
молекул Н2О (рис. 6 слева) и D2O (рис 6 справа)
качественно соответствуют экспериментальным данным.
Наблюдавшаяся в [11] модуляция кинетики есть результат усреднения по всему ансамблю молекул Н2О в области пересечения пучков накачки и зондирования. Ненулевая модуляция на частотах вращения Н2О (D2O) указывает на их синхронизацию внешним воздействием фемтосекундного импульса накачки. Фемтосекундный импульс накачки, по-видимому, частично «выстраивает» [42] диполи молекул Н2О в плоскости электрического вектора оптического пучка, запуская процесс их синхронного вращения, что и проявляется в модуляции кинетики флюоресценции.
Таким образом, включение вращательных переходов спин-изомеров Н2О (D2O), уединенных в РЦ, в квантово-механический расчет кинетики релаксации возбужденных состояний с разделёнными зарядами РЦ позволило объяснить модуляцию амплитуды, которая наблюдалась в экспериментах накачка-зондирование [9]. Поэтому предложенная нами гипотеза [1] о том, что изолированные молекулы Н2О (D2O) играют в РЦ роль вентиля, модулирующего кинетику релаксации возбужденных состояний РЦ, получила предварительное теоретическое обоснование. Полученное качественное согласие наблюдаемых [9, 10, 25] и расчетных зависимостей кинетики для обоих типов воды (см. рис.6) указывает, по нашему мнению, на адекватность разработанного теоретического подхода.
Представленные здесь результаты усиливают наше предположение о том, что именно вращающиеся молекулы Н2О (D2O) с собственным магнитным полем суммарного спина обеспечивают модуляцию кинетики населённости возбуждённого состояния P* реакционного центра пурпурных бактерий на первой стадии разделения заряда в процессах фотосинтеза. Физика изучаемого процесса близка к известному в спинтронике явлению модуляции тока (спин-зависимое рассеяние) или гигантского магнитного сопротивления в сверхрешетках [43, 44]. В нашем случае роль элемента с постоянным магнитным моментом (как в сверхрешетках) может выполнять атом негемового железа, который фиксирован вблизи вращающихся молекул воды внутри РЦ. Здесь РЦ можно считать аналогом сверхрешетки.
Работа выполнена при частичной поддержке грантов РФФИ 09-02-01173_а, 08-02-00008_а, 10-02-90301-Вьет_а, 11-02-00034-а, 12-02-31639-мол_а
Список литературы
1. S.M.Pershin and R.Y.Pishchalnikov. Physics of Wave Phenomena 20, 35 (2012).
2. R.Y.Pishchainikov, S.M.Pershin, and A.F.Bunkin. Biophysics (2012).
3. J.Deisenhofer, O.Epp, K.Miki, R.Huber, and H.Michel. Nature 318, 618 (1985).
5. B.Robert and M.Lutz. Biochemistry 27, 5108 (1988).
6. J.Deisenhofer, O.Epp, K.Miki, R.Huber, and H.Michel. Journal of Molecular Biology 180, 385 (1984).
11. V.I.Novoderezhkin, A.G.Yakovlev, R.van Grondelle, and V.A.Shuvalov. Journal of Physical Chemistry B 108, 7445 (2004).
12. J.Klein and R.Voltz. Phys. Rev. Lett 36, 1214 (1976).
14. J.Funfschilling, I.Zschokkegranacher, S.Canonica, and U.P.Wild. Helvetica Physica Acta 58, 347 (1985).
15. B.V.Trubitsin, M.D.Mamedov, L.A.Vitukhnovskaya, A.Y.Semenov, and A.N.Tikhonov. Febs Letters 544, 15 (2003).
17. S.M.Pershin. Physics of Wave Phenomena 13, 192 (2005).
21. А.Ф.Бункин, А.А.Нурматов, and С.М.Першин. Успехи физических наук 176, 883 (2006).
22. S.M.Pershin and A.F.Bunkin. Laser Physics 19, 1410 (2009).
27. Тулинов А.Ф. Успехи физических наук 87, 585 (1965).
28. Зацепина Г.Н. Журнал Структурной Химии 10, 211 (1969).
29. Golo V.L. and S.M.Pershin. Physics of Wave Phenomena 20, (2012).
30. X.Michaut, A.M.Vasserot, and L.Abouaf-Marguin. Vibrational Spectroscopy 34, 83 (2004).
32. Быков А.Д., Синица Л.Н., and Стариков В.И. Экспериментальные и теоретические методы в спектроскопии молекул водяного пара. Издательство СО РАН, Новосибирск. 1999.
33. V.A.Shuvalov, A.V.Klevanik, A.V.Sharkov, Yu.A.Matveetz, and P.G.Krukov. Febs Letters 91, 135 (1978).
34. N.Ivashin and S.Larsson. Journal of Physical Chemistry B 112, 12124 (2008).
35. D.Abramavicius, B.Palmieri, D.V.Voronine, F.Sanda, and S.Mukamel. Chemical Reviews 109, 2350 (2009).
36. D.Abramavicius and S.Mukamel. Journal of Chemical Physics 133, 6097 (2010).
37. J.K.G.Watson. Molecular Physics 15, 479 (1968).
38. Philip R.Bunker. Molecular Symmetry and Spectroscopy. Academic Press, 1979.
39. J.K.G.Watson. Molecular Physics 19, 465 (1970).
40. Shaul Mukamel. Principles of Nonlinear Optical
Spectroscopy.
41. P.L.Chapovsky and L.J.F.Hermans. Annual Review of Physical Chemistry 50, 315 (1999).
42. B.A.Zon. European Physical Journal D 8, 377 (2000).
43. R.Jansen. Journal of Physics D-Applied Physics 36, R289 (2003).
44. П.А.Грюнберг. Успехи физических наук 178, 1349 (2008).
45. R.Y.Pishchalnikov, S.M.Pershin, and A.F.Bunkin. Physics of Wave Phenomena 20, 184 (2012).
46. R.Yu.Pishchalnikov, S.M.Pershin, and A.F.Bunkin. Biophysics 57, 779 (2012).